體細胞拷貝數增加在多種癌癥類型中普遍存在,然而其在致癌發生過程中所發揮的作用目前研究人員尚未充分評估過,這部分是由于復制增益會跨越較大的染色體區域,從而就會模糊因果位點。近日,一篇發表在國際雜志Cell Reports上題為“Functional screening of amplification outlier oncogenes in organoid models of early tumorigenesis”的研究報告中,來自斯坦福大學醫學院等機構的科學家們通過研究發現了一種新方法來篩選引起多種不同類型癌癥生長的基因,并識別出了在口腔癌和食管鱗狀癌中非常有希望的潛在靶點。
文章中,研究人員利用稱之為類器官的三維器官組織模型,從癌癥基因組圖譜中識別并測試潛在的基因靶點。研究者Ameen Salahudeen博士解釋道,癌癥基因組圖譜中有大量的數據,這一領域目前已經開發出了能延長患者壽命的精準藥物,但這些數據中僅有一小部分能告訴我們癌癥是如何生長的以及是否其能作為新型藥物靶點;我們需要一種可擴展的功能性方法來從驅動癌癥生長的原因以及是否其能被靶向作用方面對數據進一步深入分析。
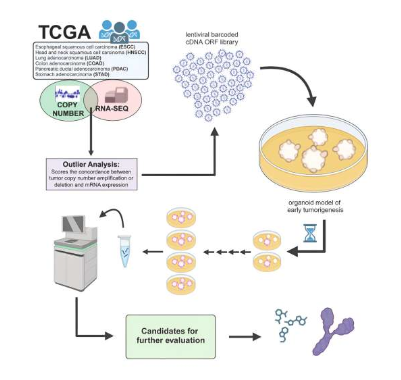
利用在培養皿中培育的類器官或能識別出驅動腫瘤生長的特殊基因。
圖片來源:Cell Reports (2023). DOI:10.1016/j.celrep.2023.113355
為了能闡明引起腫瘤生長的基因,研究人員決定重點關注能展示兩種情況的基因組區域,即具有相同基因異常高拷貝的基因組區域,這在許多癌癥類型中都非常常見;以及具有較高RNA表達水平的基因組區域,這或許表明這些基因參與到了腫瘤的生長過程中,為此研究人員利用了其所開發的新型算法來進一步研究。隨后研究人員在基因組中確定了6種不同癌癥類型的潛在區域,包括食管癌、口腔癌、結腸癌、胃癌、胰腺癌和肺癌;下一步他們為這6個器官構建了特定的腫瘤類器官,并在類器官中測試了其候選基因來觀察哪些基因與生長中的腫瘤有關。
研究人員進一步解釋道,在這一步驟中使用類器官是對此前標準方法的改進,通常在細胞癌癥研究領域所使用的永生化細胞系在實驗室生長很多年后往往會發生許多額外的突變,這或許就會讓事情變得更加糟糕混亂,在小鼠機體中測試的多種潛在基因是不可擴展的,而且測試往往還會花費數年時間。隨后研究人員利用這些基因的慢病毒文庫來篩選類器官,類器官在口腔和食道鱗狀癌中能展現出尤為有趣的研究結果,這兩種癌癥中很少有能利用藥物靶向作用的驅動基因;此外,研究人員還測試了一種名為FGFR抑制劑的臨床可用小分子在食管類器官中的作用效果,結果發現其能明顯縮小腫瘤的尺寸。
研究者Salahudeen說道,FGFR3在近一半的食管鱗狀癌中都會發生擴增,且其能與FGFR相互作用,因此這或許就能讓近一半的食管癌患者獲益。下一步研究人員將會在食管鱗狀癌患者中調查現在在臨床中使用的FGFR抑制劑在新的適應癥中的使用效果,并繼續研究研究人員所發現的其它潛在的基因。綜上,本文研究中,研究人員建立了基于類器官的候選基因組驅動子的背景篩選策略,其或能在早期腫瘤發生過程中進行一定的功能評估。
原始出處:
Ameen A. Salahudeen,Jose A. Seoane,Kanako Yuki, et al. Functional screening of amplification outlier oncogenes in organoid models of early tumorigenesis, Cell Reports (2023). DOI:10.1016/j.celrep.2023.113355





 17312606166
17312606166