2型糖尿病影響著全球5億多人。在一項新的研究中,來自美國威爾康奈爾醫學院的研究人員發現了一種在糖尿病臨床前模型中刺激健康的產生胰島素的胰腺β細胞生長的新途徑。這一發現為未來的療法帶來了希望,將改善2型糖尿病患者的生活。相關研究結果近期發表在JournalofClinicalInvestigation期刊上,論文標題為“NoncanonicalCDK4signalingrescuesdiabetesinamousemodelbypromotingβcelldifferentiation”。

論文通訊作者、威爾康奈爾醫學院代謝健康中心主任LauraAlonso博士說,“這令人欣慰,因為該領域長期以來一直認為細胞增殖會導致‘去分化’和細胞功能喪失。我們的研究結果與這一教條背道而馳,它表明,如果我們能找到一種方法來觸發體內β細胞的復制,就不會損害它們產生和分泌胰島素的能力。”
當β細胞衰竭時
2型糖尿病通常與肥胖有關,身體組織會對胰島素產生抵抗性,這意味著它們無法吸收和利用血糖。與此同時,胰腺中產生胰島素的β細胞也會衰竭---它們的數量減少,功能喪失。
Alonso博士和她的同事們在缺乏IRS2的糖尿病小鼠模型中重現了這些情況,其中IRS2是一種能允許胰島素向細胞傳遞信號以吸收血糖的蛋白。這些小鼠表現出胰島素抵抗,這是人類2型糖尿病的一個重要特征。Alonso博士說,“除此之外,IRS2蛋白對β細胞功能和β細胞數量也至關重要。”因此,它們的β細胞池已經枯竭。
拯救這些小鼠的首要任務是提高β細胞數量。但怎么做呢?她和她的團隊仔細研究了控制細胞增殖的分子機制。他們觀察到,在IRS缺陷的糖尿病小鼠體內,β細胞未能提高細胞周期蛋白D2(cyclinD2)的產量。這種蛋白與一種名為CDK4的蛋白配對后,可驅動細胞分裂。之前的研究表明,缺乏CDK4的小鼠也會患糖尿病。基于此,測試提高CDK4的活性是否有助于增加β細胞的數量似乎合乎邏輯。
β細胞增殖---數量和質量
當Alonso博士及其研究團隊通過遺傳手段為這些糖尿病小鼠引入一種CDK4活性形式(這種CDK4更容易附著在細胞周期蛋白D2上)時,他們注意到的第一件事就是它們的血糖恢復了正常。與未經治療的IRS2突變小鼠相比,它們的β細胞數量更多了。
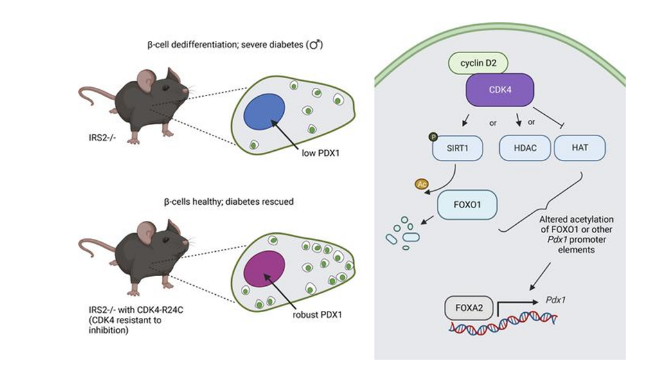
Alonso博士生說,不過更好的是“這些經過治療的小鼠的β細胞看起來非常健康,而原來的糖尿病小鼠的β細胞看起來非常糟糕。提高CDK4的活性能使β細胞充滿胰島素。”這支持了在不影響功能的情況下擴大β細胞數量的概念。
雖然CDK4本身并不是一種可行的治療靶點,因為它刺激細胞增殖的能力可能會增加患癌癥的風險,但是Alonso博士相信,探究支配β細胞分裂和功能的分子通路總有一天可能會帶來臨床突破。她提到了索馬魯肽(Ozempic),這是最受關注的抗糖尿病新藥物之一。
Alonso博士說,“這種藥物是一位科學家在研究吉拉毒蜥(Gilamonster)唾液中的毒素時發現的。因此,很明顯,了解基本生物學的工作原理可以在治療甚至預防糖尿病方面帶來真正的進步。”





 17312606166
17312606166