目前,日益嚴重的肥胖流行病對全球健康的威脅正在擴大。與肥胖相關的代謝功能障礙是長期心血管并發癥的危險因素,這突出了肥胖對人群健康的主要影響。營養過剩,尤其是缺乏體育活動,是肥胖和糖尿病發病的主要原因。因此,熱量限制和運動訓練等生理干預措施已被證明在預防和治療代謝紊亂方面發揮了各種有益作用。
盡管有這些見解,人們對運動有益的理解仍然有限。特別是,肌肉功能、局部免疫反應的調節和運動之間的分子聯系目前基本上還不明確。這種知識差距與肌肉局部免疫調節的影響及其與肌肉完整性、功能和再生的相互作用有關。因此,解剖肌肉特異性免疫調節以及肌肉功能、適應和再生,對于未來推進免疫調節的小生境特異性靶向干預至關重要。

圖片來源:https://doi.org/10.1016/j.cmet.2023.08.010
近日,來自德國亥姆霍茲國家研究中心的研究者們在Cell Metab.雜志上發表了題為“Regulatory T cells require IL6 receptor alpha signaling to control skeletal muscle function and regeneration”的文章,肌肉損傷模型表明,IL6Ra TKO小鼠在肌肉再生方面有顯著的障礙。Treg功能的獲得可恢復IL6Ra TKO小鼠受損的肌肉修復。
從免疫學的角度來看,研究者最近在骨骼肌中發現了一種特定的組織調節性T細胞群(Tregs),其顯示出不同的T細胞受體(TCR)庫和特定的轉錄組。Tregs的特征是CD4、CD25和轉錄因子Foxp3的表達,Foxp3是Tregs發育和功能的主要調節因子。與淋巴組織中的Treg相反,非淋巴組織(如肌肉)中的Tregs在控制和維持組織穩態、完整性和功能方面發揮著關鍵作用。肌肉Tregs具有高表達水平的兩調節蛋白(Areg),表皮生長因子家族的成員,其受體(表皮生長因子受體EGFR)在肌肉內的免疫細胞和衛星細胞(SC)上表達。Areg最近被證明在協調宿主抵抗和容忍機制方面發揮著核心作用。
在這里,研究者發現運動促進了高功能性肌肉分泌Tregs的穩定誘導,同時增加了兩調節蛋白(Areg)、EGFR和ST2的表達。從機制上講,研究者發現T細胞(TKO)缺乏IL6Ra的小鼠的肌肉Treg功能以及肌肉再生所需的衛星和纖維成脂祖細胞顯著減少。使用運動和少肌癥模型,IL6Ra TKO小鼠表現出Tregs缺陷、功能成熟和肌肉質量更明顯的下降。肌肉損傷模型表明,IL6Ra TKO小鼠在肌肉再生方面有顯著的障礙。Treg功能的獲得可恢復IL6Ra TKO小鼠受損的肌肉修復。
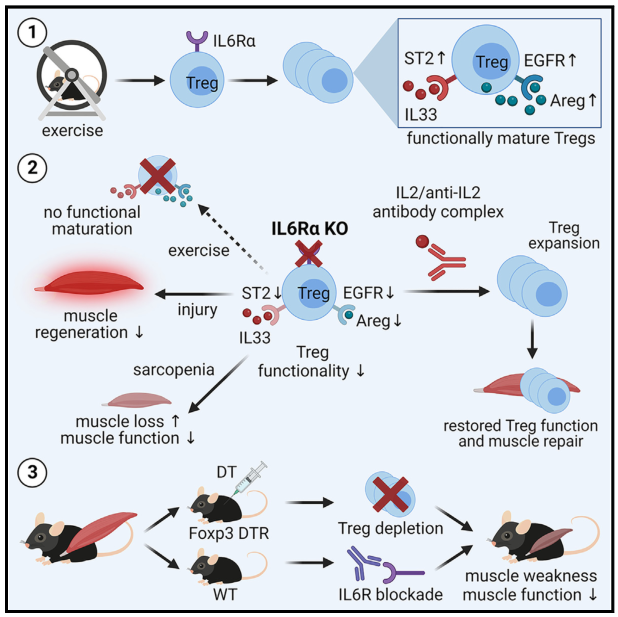
調節性T細胞需要IL6受體α信號傳導來控制骨骼肌功能和再生
圖片來源:https://doi.org/10.1016/j.cmet.2023.08.010
綜上所述,T細胞上IL6Ra的表達是介導Treg對肌肉功能、適應和修復的控制的分子界面。鑒于抗IL6R治療與肌無力發展的相關性,所提出的研究結果具有臨床相關性。Tregs在非淋巴組織中的功能特化,保證了未來應用策略的優化,這將允許對這些相關免疫細胞進行小生境和/或環境特異性靶向。





 17312606166
17312606166