近年來(lái),基于胚胎干細(xì)胞體外構(gòu)建的“類(lèi)囊胚”、“類(lèi)原腸胚”以及“軀干樣結(jié)構(gòu)”等胚胎類(lèi)似模型[1-3],幫助人們更加深入地理解脊椎動(dòng)物形態(tài)發(fā)生的機(jī)制,同時(shí)也為研究發(fā)育相關(guān)疾病提供了補(bǔ)充模型。目前,這些體外模型能夠重現(xiàn)和模擬體內(nèi)重要的發(fā)育生物學(xué)事件,例如:體軸建立、胚層分化和細(xì)胞的定向運(yùn)動(dòng)等。然而,目前尚沒(méi)有較好的方法在體外誘導(dǎo)出脊椎動(dòng)物較為完整的頭部結(jié)構(gòu),其可能的原因是目前的模型都未能充分模擬原腸運(yùn)動(dòng)過(guò)程中一些非常重要的發(fā)育學(xué)事件,例如:胚孔的形成和中內(nèi)胚層的內(nèi)卷運(yùn)動(dòng),這些過(guò)程對(duì)于神經(jīng)外胚層的正確誘導(dǎo)和圖式形成發(fā)揮重要的功能。
2023年4月4日,浙江大學(xué)醫(yī)學(xué)院徐鵬飛團(tuán)隊(duì)與哈佛大學(xué)醫(yī)學(xué)院Sean G. Megason團(tuán)隊(duì)合作,在Cell Reports上發(fā)表題為"Nodal coordinates the anterior-posterior patterning of germ layers and induces head formation in zebrafish explants" 的研究論文,報(bào)道了利用斑馬魚(yú)胚胎干細(xì)胞體外構(gòu)建一個(gè)頭部類(lèi)似結(jié)構(gòu)。

徐鵬飛團(tuán)隊(duì)之前的研究報(bào)道在斑馬魚(yú)胚胎動(dòng)物極頂?shù)哪遗呒?xì)胞或者是斑馬魚(yú)胚胎外植體(Explant)中構(gòu)建Nodal和Bmp兩種形態(tài)發(fā)生素(Morphogen)的濃度梯度能夠誘導(dǎo)一個(gè)完整的胚胎體軸[4],但是這兩種形態(tài)發(fā)生素各自發(fā)揮什么功能仍不清楚。在小鼠胚胎干細(xì)胞團(tuán)中構(gòu)建BMP4的濃度梯度,細(xì)胞團(tuán)會(huì)發(fā)育成類(lèi)似于神經(jīng)發(fā)生時(shí)期的小鼠胚胎,但缺乏腦部組織,尤其是前腦[5]。在本研究中,研究人員在斑馬魚(yú)外植體中構(gòu)建Nodal信號(hào)的濃度梯度,通過(guò)活體成像技術(shù)和Imaris定量分析,發(fā)現(xiàn)Nodal會(huì)誘導(dǎo)外植體產(chǎn)生胚胎原腸運(yùn)動(dòng)時(shí)期關(guān)鍵的細(xì)胞運(yùn)動(dòng),集中延伸運(yùn)動(dòng)和內(nèi)卷運(yùn)動(dòng)(圖1)。
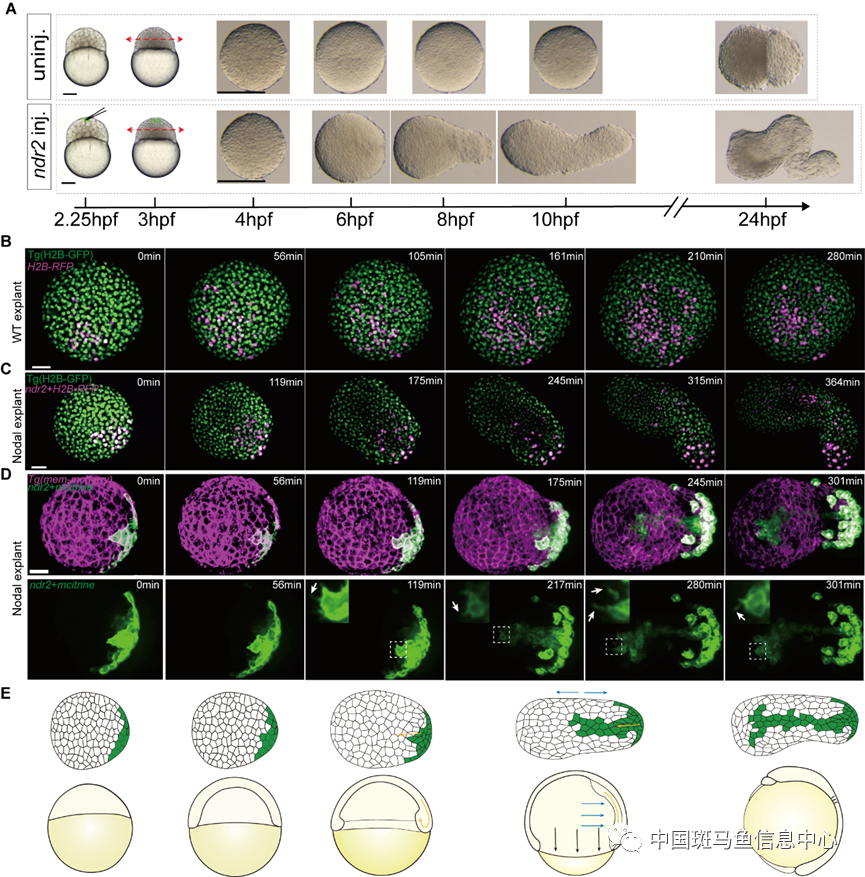
圖1 Nodal在斑馬魚(yú)外植體中誘導(dǎo)集中延伸運(yùn)動(dòng)和內(nèi)卷運(yùn)動(dòng)。
研究人員繼續(xù)通過(guò)單細(xì)胞轉(zhuǎn)錄組測(cè)序和原位雜交技術(shù),構(gòu)建了從原腸前期到器官生成時(shí)期Nodal外植體的細(xì)胞分子和空間圖示的高分辨動(dòng)態(tài)圖譜。通過(guò)進(jìn)一步分析發(fā)現(xiàn):Nodal誘導(dǎo)的中內(nèi)胚層細(xì)胞,包括:前部?jī)?nèi)胚層、前脊索板、脊索以及類(lèi)尾牙位于外植體中間沿著前-后軸依次排列。令人驚奇的是位于外植體外圍的神經(jīng)外胚層細(xì)胞同樣沿著前-后軸依次特化為前腦、中腦、后腦和脊髓。Nodal外植體在原腸運(yùn)動(dòng)時(shí)期逐步發(fā)育成一個(gè)頭部類(lèi)似結(jié)構(gòu)(Head Like Structure)(圖2)。
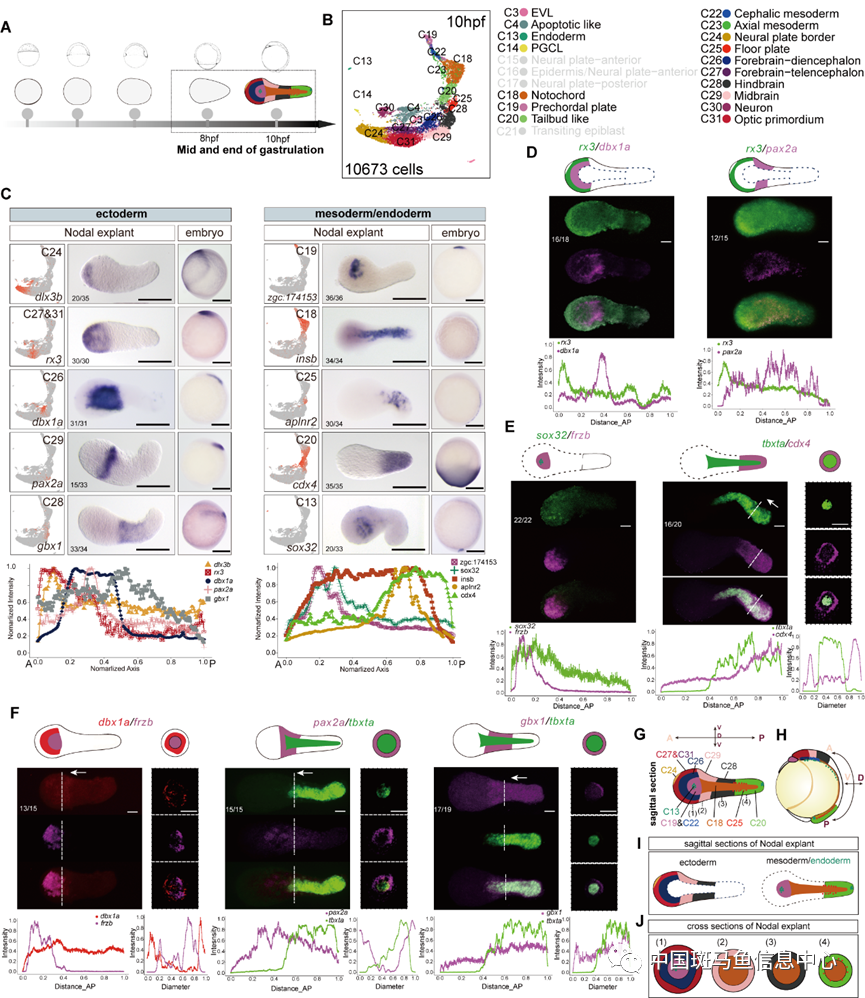
圖2 Nodal外植體原腸末期(10 hpf)細(xì)胞分子和空間圖式圖譜
通過(guò)bulk RNAseq和腹側(cè)過(guò)表達(dá)實(shí)驗(yàn),研究人員解析了Nodal發(fā)揮“組織者”功能的分子基礎(chǔ),他們篩選得到105個(gè)Nodal下游靶基因,其中有14個(gè)基因具有第二體軸誘導(dǎo)能力,其中5個(gè)基因能夠誘導(dǎo)完整或部分的頭部結(jié)構(gòu)(圖3)。
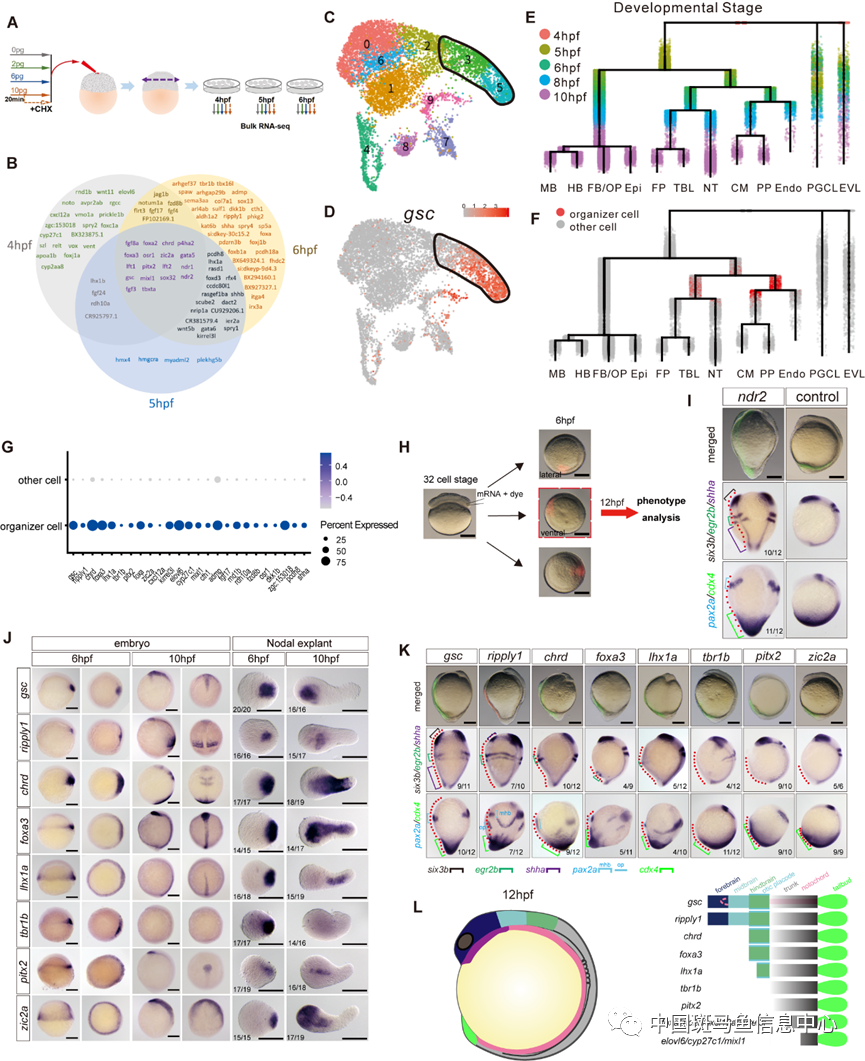
圖3 Nodal發(fā)揮“組織者”功能的分子基礎(chǔ)
此項(xiàng)研究不僅幫助我們進(jìn)一步理解脊椎動(dòng)物的頭部發(fā)育,更重要的是,為體外誘導(dǎo)脊椎動(dòng)物頭部發(fā)生提供了可行的策略,這將為更進(jìn)一步研究脊椎動(dòng)物頭部發(fā)育和相關(guān)疾病提供了一個(gè)優(yōu)良的模型。同時(shí),這項(xiàng)工作提供了大量的轉(zhuǎn)錄組數(shù)據(jù)和原位雜交數(shù)據(jù),為我們進(jìn)一步解析脊椎動(dòng)物胚胎發(fā)育過(guò)程中胚層分化的分子機(jī)制、頭部圖式形成以及Nodal下游的信號(hào)通路提供了寶貴的數(shù)據(jù)資源。這些體外類(lèi)胚胎技術(shù)的成熟與進(jìn)步將會(huì)進(jìn)一步推進(jìn)器官移植和再生醫(yī)學(xué)的發(fā)展。
浙江大學(xué)徐鵬飛教授和美國(guó)哈佛大學(xué)醫(yī)學(xué)院Sean G. Megason教授為本文的共同通訊作者,浙江大學(xué)醫(yī)學(xué)院程濤博士和邢延奕博士為論文的共同第一作者。該研究受到科技部重點(diǎn)研發(fā)計(jì)劃、國(guó)家自然科學(xué)基金等項(xiàng)目的資助。該工作致敬著名的發(fā)育生物學(xué)家Bernard Thisse教授(1959-2021)。研究過(guò)程中還受到弗吉尼亞大學(xué)Christine Thisse教授,浙江大學(xué)馬駿教授、楊小杭教授和管敏鑫教授的大力支持。
參考文獻(xiàn):
1. Beccari, L., Moris, N., Girgin, M., Turner, D.A., Baillie-Johnson, P., Cossy, A.C., Lutolf, M.P., Duboule, D., and Arias, A.M. (2018). Multi-axial self-organization properties of mouse embryonic stem cells into gastruloids. Nature 562, 272-276. 10.1038/s41586-018-0578-0.
2. Moris, N., Anlas, K., van den Brink, S.C., Alemany, A., Schroder, J., Ghimire, S., Balayo, T., van Oudenaarden, A., and Martinez Arias, A. (2020). An in vitro model of early anteroposterior organization during human development. Nature 582, 410-415. 10.1038/s41586-020-2383-9.
3. Veenvliet, J.V., Bolondi, A., Kretzmer, H., Haut, L., Scholze-Wittler, M., Schifferl, D., Koch, F., Guignard, L., Kumar, A.S., Pustet, M., et al. (2020). Mouse embryonic stem cells self-organize into trunk-like structures with neural tube and somites. Science (New York, N.Y.) 370. 10.1126/science.aba4937.
4. Xu, P.F., Houssin, N., Ferri-Lagneau, K.F., Thisse, B., and Thisse, C. (2014). Construction of a vertebrate embryo from two opposing morphogen gradients. Science (New York, N.Y.) 344, 87-89. 10.1126/science.1248252.
5. Xu, P.F., Borges, R.M., Fillatre, J., de Oliveira-Melo, M., Cheng, T., Thisse, B., and Thisse, C. (2021). Construction of a mammalian embryo model from stem cells organized by a morphogen signalling centre. Nature communications 12, 3277. 10.1038/s41467-021-23653-4.





 17312606166
17312606166 加微信獲取對(duì)接
加微信獲取對(duì)接